LPG
(Liquified Petroleum Gas) merupakan gas alam yang dicairkan dan dikemas dalam
tabung kedap udara dan kuat, ketika tekanan dalam tabung berkurang maka cairan
itu akan berubah menjadi gas kembali. Bagaimana suatu gas dapat menjadi cair?
Gambar 2.10 tabung
berisi LPG
Suatu zat
dalam fasa gas, pada suhu tinggi dan tekanan yang relative rendah di atas titik
didihnya, molekul-molekulnya berdiri sendiri. Tetapi, ketika suhu diturunkan
dan tekanan dinaikkan hampir mendekati titik embunnya, maka terjadilah gaya
tarik menarik antarmolekul yang menyebabkan suatu gas dapat berubah menjadi
cair.
Gaya
antarmolekul merupakan gaya yang terjadi di antara molekul-molekul unsur atau
senyawa yang menyebabkan molekul-molekul tersebut mengadakan tarik menarik
dengan kekuatan tertentu. Ada dua jenis gaya antarmolekul yang akan dibahas
pada diktat ini, yaitu: gaya van der
waals dan ikatan hidrogen.
1. Gaya van der waals
Kekuatan gaya van der waals lebih lemah dibandingkan ikatan kovalen atau ikatan
ion dan sangat dipengaruhi oleh kepolaran dari masing-masing molekul. Gaya ini
bekerja jika jarak antar molekul sudah dekat dan tidak melibatkan terjadinya
pembentukan ikatan antar atom.
Ada tiga gaya yang
menyusun gaya van der waals, yaitu:
a. Gaya orientasi
Gaya ini terjadi antardipol
permanen pada molekul-molekul polar seperti HCl, HBr, dan HI. Gaya antardipol
disebabkan karena adanya gaya tarik menarik antara dipol positif atom dalam
suatu molekul dengan dipol negative atom pada molekul lainnya. Contoh
antarmolekul polar HCl, seperti ditunjukkan pada gambar 2.11
Gambar 2.11. gaya antar dipol pada HCl
b. Gaya induksi
Gaya ini
terjadi akibat adanya gaya tarik menarik antara dipol permanen pada molekul
polar dengan dipol sesaat pada molekul nonpolar. Dipol sesaat pada molekul
nonpolar terjadi akibat adanya imbasan atau induksi dari molekul-molekul polar
pada molekul nonpolar, sehingga elektron-elektron dari molekul nonpolar
tersebut terkumpul pada salah satu kutub yang menyebabkan terbentuknya dipol
sesaat pada molekul nonpolar. Contoh gaya antar molekul polar (H2O)
dengan molekul non polar Cl2
c.
Gaya dispersi (gaya London)
Gaya dispersi
atau disebut dengan gaya London karena dikemukakan oleh Fritz London pada tahun
1928. Gaya ini terjadi antara dipol sesaat molekul-molekul nonpolar atau
atom-atom gas mulia. Dipol sesaat ini terjadi karena adanya pergerakan elektron
pada molekul nonpolar atau atom gas mulia. Jika suatu waktu elektron tersebut
ditemukan dibagian ujung molekul, maka akan membentuk dipol negative. Sementara
pada bagian yang lain akan mengalami kekurangan elektron akan membentuk dipol
positif. Dipol sesaat yang terbentuk akan mengimbas pada molekul disekitarnya,
sehingga membentuk suatu dipol terimbas. Kemudahan suatu molekul untuk
membentuk dipol sesaat atau untuk mengimbas suatu molekul disebut
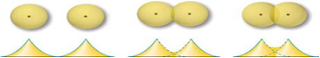
polarisabilitas. Contoh gaya dispersi adalah gaya antar molekul F2,
seperti pada gambar 2.12
Gambar 2.12. gaya dispersi
antar molekul F2
Gaya dispersi dapat
mempengaruhi titik leleh dan titik didih suatu molekul berdasarkan mudah atau
tidaknya molekul tersebut mengalami polarisasi.
Kemampuan
polarisasi ditentukan oleh jumlah elektron dan bentuk molekulnya. Misalnya
radon mempunyai titik didih lebih tinggi dibandingkan dengan helium karena
massa atom relatif radon lebih besar dibandingkan helium. Hal ini meyebabkan
jumlah elektron pada argon lebih besar dan jari-jarinya atom lebih panjang
sehingga argon mudah mengalami polarisasi.
Pengaruh
bentuk molekul terjadi pada normal pentana (titik didih 360) dibandingkan
dengan dengan 2,2-dimetilpropana (titik
didih 100C). Hal ini terjadi karena normal pentana mempunyai
struktur lurus sedangkan 2,2-dimetilpropana mempunyai struktur bercabang.
Adanya rantai lurus menyebabkan gaya tarik molekul-molekul pada pentana menjadi
lebih efektif.
2. Ikatan hidrogen
Titik didih senyawa
hidrida dari unsur-unsur golongan IVA, VA, VIA, dan VIIA ditunjukkan pda grafik
berikut:
Pada kurva titik
didih senyawa hidrida golongan IVA (group 14), ternyata titik didih meningkat
sesuai dengan semakin besar massa molekul relatifnya. Hal ini dikarenakan
semakin besar massa atom relatifnya maka gaya van der Waals juga makin kuat
sehingga dibutuhkan energi yang lebih besar untuk melepaskan ikatan yang
terjadi akibat gaya tersebut.
Akan tetapi, untuk
kurva titik didih senyawa hidrida golongan VA (group 15), VIA (group 16), dan
VIIA (group 17) terdapat perbedaan pada titik didih HF, H2O, dan NH3.
Ketiga senyawa itu mempunyai titik didih lebih tinggi dari hidrida lainnya
walaupun massa molekul relatifnya lebih kecil. Hal ini menunjukkan bahwa ada
gaya tarik menarik antarmolekul yang sangat kuat dalam senyawa tersebut. Gaya
tersebut diakibatkan adanya ikatan hidrogen. Ikatan hidrogen terjadi karena
dalam ikatan H-F, H-O, dan H-N dimana unsur F, O, dan N sangat elektronegatif
sedangkan atom H sangat elektropositif. Akibatnya, atom H dari satu molekul
akan terikat kuat pada atom unsur (F, O, atau N) dari molekul lain melalui
pasangan elektron bebas atom unsur tersebut.
Ikatan hidrogen
adalah ikatan yang terjadi antara atom yang sangat elektronegatif pada suatu
molekul dengan atom Hidrogen dari molekul yang lain.
Contoh ikatan hidrogen antarmolekul HF
seperti pada gambar 2.13. garis (…..) menunjukkan ikatan hidrogen.
Gambar 2.13. ikatan hidrogen antar molekul
HF
Molekul yang mempunyai ikatan hidrogen akan
mempunyai titik didih relative lebih tinggi dibandingkan molekul yang memiliki
gaya van Der Waals. Misalnya
1-propanol mempunyai titik didih 970C dan etil metil eter mempunyai
titik didih 80C.
Beberapa contoh ikatan hidrogen terdapat
pada gambar 2.14.
Gambar 2.14. ikatan hidrogen antar HF, air
dan etanol, antar asam salisilat, antar asam formiat, antara ammonia dan air,
dan antar glisin.